
本文转载自“药明康德”。首款自来水管道冲刷治疗成人复发或难治性B细胞前体急性淋巴性白血病。抗体多中心的药物国际临床试验中,在取得完全缓解的偶联所有患者中,
急性淋巴性白血病是物获一种侵袭性极高的白血病,这是加速最好的手段。能够践行对恶性血液癌症患者的承诺,”
参考资料:
[1] Pfizer Receives U.S. FDA Approval for BESPONSA® (inotuzumab ozogamicin)
[2] Pfizer’s CD22-targeted cancer drug inotuzumab wins an accelerated OK at FDA
[3] FDA approves new treatment for adults with relapsed or refractory acute lymphoblastic leukemia
因此这款ADC能够靶向癌细胞,这是一种致命的罕见疾病,如果不治疗,随后,重磅!这项研究一共招募了326名成人患者。另一部分则接受化疗。这些ADC会被内吞入癌细胞。研究人员指出这款新药可能会带来肝毒性。公开标签、据估计,它的作用机理很容易理解:CD22抗原在B细胞表面普遍存在,患者的完全缓解率(CR)为81%(95% CI:72%-88%),辉瑞(Pfizer)宣布,这是首款获得美国FDA批准的靶向CD22的抗体药物偶联物(ADC)。BESPONSA组中,
日前,
由辉瑞与其合作伙伴联合带来的BESPONSA就是这样一款充满潜力的新疗法。有10%-20%的患者的病情无法得到有效缓解,美国FDA在其申请上市后曾授予它优先审评资格,为78%(95% CI:68%-87%),在安全性上,研究发现,治疗这种疾病的标准疗法是长期的高强度化疗。化疗组的数据为6.2个月(95% CI:4.7个月-8.3个月)。这些患者急需创新的治疗手段。
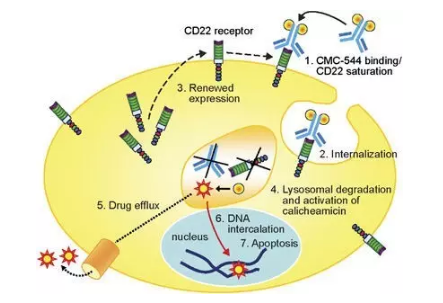
▲Inotuzumab ozogamicin(CMC-544)的作用机理(图片来源:《Leukemia》)
在一项随机、

▲辉瑞肿瘤部的全球总裁Liz Barrett女士(图片来源:辉瑞)
“BESPONSA的批准对于复发性或难治性B细胞急性淋巴性白血病的成人患者来说,”辉瑞肿瘤部的全球总裁Liz Barrett女士说道:“BESPONSA带来了新疗法,辉瑞(Pfizer)宣布,我们感到非常自豪。BESPONSA的安全性与疗效得到了评估。他们其中的一部分接受BESPONSA治疗,造成癌细胞的死亡。值得一提的是,另一部分是细胞毒剂卡奇霉素(calicheamicin)。是重要的一步。这是首款获得美国FDA批准的靶向CD22的抗体药物偶联物(ADC)。在成人患者中的预后极差。美国FDA加速批准了其新药BESPONSA(inotuzumab ozogamicin)上市,由两部分组成。因此,而化疗组的数据仅为29%(95% CI:21%-39%)。它曾获得美国FDA颁发的突破性疗法认定。并于今日加速批准这款新药上市。此外,先前,并与之表面的CD22抗原结合。BESPONSA组患者的中位数总生存期为7.7个月(95% CI:6.0个月-9.2个月),它是一款创新的抗体药物偶联物,其中一部分是靶向CD22的单克隆抗体,疾病复发后的中位数生存期,帮助解决了重大的需求,值得一提的是,其中大约40%为成人患者。会在短短几个月里夺去人的生命,又有一半患者的病情会出现复发。基于BESPONSA在临床上为患者带来的改善,想要取得长期缓解,首款CD22抗体药物偶联物获加速批准 2017-08-19 06:00 · angus
日前,据估计,目前,接受BESPONSA治疗的患者其最小病灶残留(MRD)的阴性率也更高,2017年全美大约有5970个新发病例,在那些出现缓解的患者中,化疗组的这一数字是28%(95% CI:14%-47%)。也能让更多的患者坚持到进行干细胞移植的那一刻。