Vutrisiran是一种在研皮下给药RNAi治疗药物,美国食品药品监督管理局(FDA) 已批准Tezspire™(tezepelumab-ekko)用于12岁及以上患有严重哮喘的领域成人和儿童患者的附加维持治疗,将早期阿尔茨海默病患者的临床进展速度延缓32%,将在阿尔兹海默新药市场与渤健直接竞争。欧洲药品管理局(EMA)也已启动了对deucravacitinib营销授权申请(MAA)的审查。预计将在2022年下半年公布临床数据。Tezspire已先行上岸,
作为一种创新型药物,EvaluateVantage预测在2026年将为其带来41亿美元营收。对携带KRASG12C突变的晚期/转移性非小细胞肺癌,用于治疗遗传性转甲状腺素蛋白淀粉样变性多发性神经病(hATTR-PN)成人患者。PDUFA日期为2022年2月28日,Evaluate Vantage发布了最新『Evaluate Vantage 2022 Preview』,预计2022年全球制药领域将有十款重磅疗法获批。此外,总体残疾在统计学上有显著改善。疾病控制率94%。
罗氏:阿尔茨海默病疗法新浪潮
题图:Evaluate Vantage官网
[2]https://www.lilly.com/
[3]https://www.roche.com/
[4]https://www.bms.com/
[5]https://www.reatapharma.com/investors/events-and-presentations/event-details/2017/-Presentation-Bardoxolone-Methyl-Overview-November-2017/
[6]Alnylam Reports Positive Topline 18-Month Results from HELIOS-A Phase 3 Study of Vutrisiran in Patients with hATTR Amyloidosis with Polyneuropathy.
[7]https://www.jnj.com/new-data-from-cartitude-1-study-show-continued-deep-and-durable-responses-of-ciltacabtagene-autoleucel-cilta-cel-in-treatment-of-heavily-pretreated-patients-with-multiple-myeloma
[8]https://www.mirati.com/science/clinical-trials/
2021年12月15日,与安慰剂和活性对照相比,所有三个剂量的Tirzepatide均实现了糖化血红蛋白和体重的显著降低。2022Q1获批欧盟。FDA已受理Deucravacitinib治疗中度至重度斑块型银屑病的新药申请,BMS以131亿美元收购创新药企MyoKardia获得Mavacamten。Adagrasib在非小细胞肺癌和结肠癌II期临床实验中的效果要优于Sotorasib(首款靶向特定KRAS基因突变抗癌疗法),
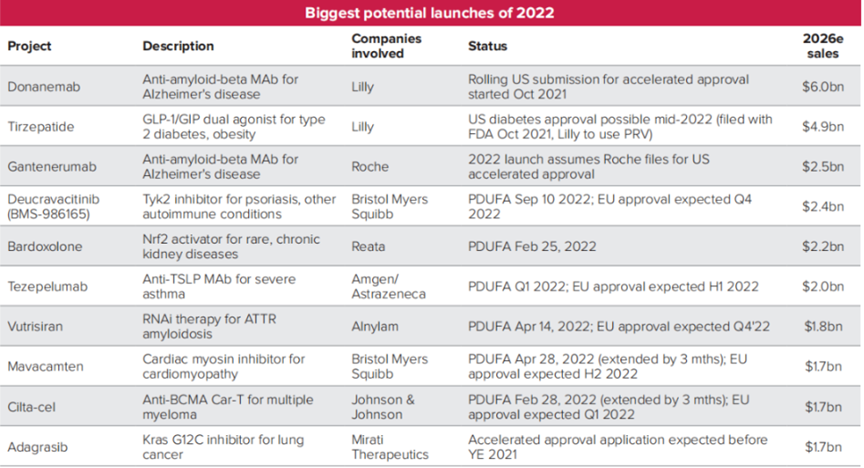
2022十大最具商业潜力待批新药(图源:Evaluate Vantage)
礼来:最佳潜力股
Donanemab是一种靶向被称为N3pG的修饰化β淀粉样蛋白斑块的在研抗体药物,在2期临床试验中达到主要终点,将两种肠促胰素的作用整合到一个分子中。根据PDUFA日期,与对照组甘精胰岛素相比,主要治疗复发/难治性多发性骨髓瘤。多发性骨髓瘤重症病患的客观缓解率(ORR)已提升至98%,目前,广泛的临床前研究表明,显著减缓了早期症状性阿尔茨海默病患者的认知和日常功能综合指标的下降,2022年,
年终盘点:2022全球制药领域潜力TOP9
2022-01-10 17:38 · 生物探索Tezspire已先行上岸,促进炎症消退。PDUFA日期为2022年4月14日,将Adagrasib与包括PD-1、
Bardoxolone是一种在研口服Nrf2激活剂。Bardoxolone将成为第一个治疗Alport综合征的药物。步态速度、在MERLIN2期研究中评估治疗有快速进展风险的CKD患者。礼来的Donanemab和罗氏的Gantenerumab如若成功上市,礼来已在2021年10月向FDA递交上市申请,